Ponto de Fusão e Ebulição
Lista de 10 exercícios de Química com gabarito sobre o tema Ponto de Fusão e Ebulição com questões de Vestibulares.
Você pode conferir as videoaulas, conteúdo de teoria, e mais questões sobre o tema Ponto de Fusão e Ebulição .
01. (UFRN) O cientista russo A.M. Butlerov estudou as relações entre a composição, a estrutura e as propriedades das substâncias. Um de seus trabalhos foi a síntese do isobutano, mostrando a diferença entre algumas propriedades desse composto e as correspondentes do n-butano.
Apesar de ambos possuírem a mesma composição química, eles apresentam temperatura de ebulição diferente, como mostra o quadro abaixo:
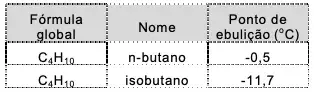
Os compostos acima são
- tautômeros.
- homólogos.
- enantiômeros.
- isômeros.
02. (UFMG) Considere as substâncias:
I. CH3(CH2)3CH3
II. CH3(CH2)3CH2OH
III. CH3CH2CH3
IV. CH3CH2OCH2CH2CH3
A alternativa que apresenta as substâncias em ordem crescente de temperatura de ebulição é:
- I, III, II, IV.
- III, I, II, IV.
- I, III, IV, II.
- III, I , IV, II.
03. (PUC-SP) Sobre os compostos butano, 1-butanol e ácido butanoico, foram feitas as seguintes afirmações:
Suas fórmulas moleculares são respectivamente C4H10, C4H10O e C4H8O2.
(II) A solubilidade em água do butano é maior do que a do 1-butanol.
(III) O ponto de ebulição do ácido butanoico é maior do que o do 1-butanol.
(IV) O ponto de fusão do butano é maior do que o ácido butanoico.
Estão corretas as afirmações:
- I, III e IV.
- II e IV.
- I e III.
- III e IV.
- I e II.
04. (PUC-SP) As propriedades das substâncias moleculares estão relacionadas com o tamanho da molécula e a intensidade das interações intermoleculares. Considere as substâncias a seguir, e suas respectivas massas molares.
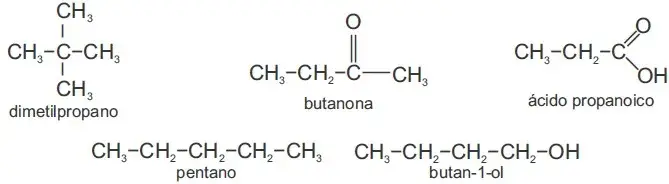
A alternativa que melhor associa as temperaturas de ebulição com as substâncias é:
05. (UESB) Ao se determinar o ponto de ebulição, ao nível do mar de uma amostra de etanol completamente incolor, foi encontrado um valor maior que o de um manual de Física e Química.
A análise do resultado obtido na determinação do ponto de ebulição do etanol permite corretamente afirmar:
- O vapor desprendido da amostra, durante a determinação, tem composição diferente do etanol analisado.
- A quantidade de etanol é menor que a necessária para a determinação do ponto de ebulição.
- A determinação do ponto de ebulição foi efetuada à pressão maior que a atmosfera
- O etanol da amostra é um líquido puro.
- A amostra de etanol contém impurezas dissolvidas.
06. (FATEC) A fórmula estrutural do composto orgânico com menor ponto de ebulição presente na tabela dada é
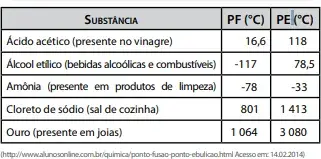
- H3C – CHO
- HCOO – CH3
- H3C – COOH
- H3C – O – CH3
- H3C – CH2 – OH
07. (UFPA) Analise as afirmativas a seguir sobre a estrutura e as propriedades dos compostos de carbono e assinale a alternativa correta.
- A acidez do composto CH3–NH2 é maior do que a acidez do composto CCl3–COOH.
- O caráter ácido dos fenóis é mais fraco do que o dos álcoois.
- O ponto de ebulição do benzeno é maior do que o ponto de ebulição do tolueno.
- O ponto de ebulição do 2-metil-heptano é maior do que o ponto de ebulição do tetrametil-butano.
- O ponto de ebulição do ciclobutano é maior do que o ponto de ebulição do ciclopentano.
08. (PUC-PR) A temperatura de fusão e de ebulição e o estado físico dos compostos orgânicos dependem fundamentalmente das forças intermoleculares e do tamanho das moléculas (massa molecular). Os compostos apresentados a seguir apresentam temperaturas de fusão e de ebulição distintas, em função do tipo de interações presentes em cada um deles.
I. CH4
II. CH3Cℓ
III. CH3OH
IV. HCOOH
Dado esse contexto, é CORRETO afirmar:
- A substância I, por ser um hidrocarboneto, é uma molécula apolar e sua temperatura de fusão de ebulição é maior que a temperatura de fusão e de ebulição da substância III, que é um álcool e apresenta interações mais fracas.
- A substância IV apresenta o maior ponto de fusão e de ebulição, pois, além de formar pontes de hidrogênio duplas entre duas moléculas, origina um dímero, aumentando ainda mais sua temperatura de fusão e de ebulição.
- A substância II é uma molécula apolar, suas interações são as mais fracas, conferindo a menor temperatura de fusão e de ebulição.
- Como todas as substâncias citadas são compostos orgânicos que apresentam o mesmo número de carbonos , as temperaturas de fusão e de ebulição são praticamente iguais.
- A substância III é um álcool e apresenta interações do tipo pontes de hidrogênio, o que faz com que sua temperatura de fusão e de ebulição seja a maior de todos os compostos.
09. (UESB) A adição de etilenoglicol, HOCH2CH2OH, à água do sistema de arrefecimento de automóveis é utilizada para evitar o congelamento durante o inverno e a produção de vapor com o superaquecimento da água.
A análise dessas informações permite concluir:
- A solução preparada com a adição de etilenoglicol, à água, possui temperatura de ebulição e de fusão superiores à da água pura.
- A pressão de vapor da solução de etilenoglicol é menor do que a da água pura, o que acarreta diminuição do ponto de ebulição desse líquido.
- A solução de arrefecimento evapora ao passar pelo radiador, o que possibilita a diminuição de temperatura desse líquido durante o funcionamento do motor.
- A adição de etilenoglicol à água causa a diminuição do calor específico desse líquido e, consequentemente, o decréscimo dos pontos de ebulição e de fusão da solução.
- O aditivo diminui a pressão de vapor da solução, quando comparada à da água pura, fazendo com que a temperatura de ebulição do líquido aumente e a temperatura de fusão diminua.
10. (UFGD) Assinale a alternativa que apresenta a substância química com menor ponto de ebulição.
- CH3COOH
- NaCl
- CH3CH2OH
- CH3CH2CH3
- H2O



