Distribuição Eletrônica II
Lista de 16 exercícios de Química com gabarito sobre o tema Distribuição Eletrônica II com questões de Vestibulares.
Você pode conferir as videoaulas, conteúdo de teoria, e mais questões sobre o tema Distribuição Eletrônica II.
01. (CESMAC) O vanádio, na forma de pó metálico, pode causar mal-estar, entre outros sintomas. Além disso, a exposição prolongada ao vanádio pode deixar a língua da pessoa contaminada com a cor azul. Com relação ao vanádio, na sua forma elementar, sua distribuição eletrônica nos orbitais atômicos pode ser expressa como:
Dados: vanádio Z = 23.
- 1s², 2s², 2p⁶, 3s², 3p⁶, 3d³, 4s²
- 1s², 2s², 3s², 2p⁶, 3p⁶, 3d³, 4s²
- 1s², 2s², 3s², 4s², 1p⁶, 2p⁶, 3p³
- 1s², 2s², 2p⁶, 3s², 3p⁶, 4s², 3d³
- 1s², 1p6, 2s², 2p⁶ 3s², 3p5
Resposta: D
Resolução: Vanádio tem número atômico Z = 2 . Sua configuração eletrônica correta é: 1s², 2s², 2p⁶, 3s², 3p⁶, 4s², 3d³.
02. (CEFET-PR) O subnível mais energético do átomo de um elemento é o 5p³, portanto, o seu número atômico e sua posição na tabela periódica serão, respectivamente:
- 15, 3° período e coluna 5 A.
- 51, 5° período e coluna 5 A.
- 51, 3° período e coluna 3 A.
- 49, 5° período e coluna 3 A.
Resposta: B
Resolução: O subnível mais energético do átomo é o 5p³, o que indica número atômico 51. O elemento pertence ao 5º período e à coluna 5A. 51, 5º período e coluna 5A.
03. (UEA - SIS) Analise os dados para responder à questão.
A tabela apresenta dados de número atômico, número de massa e quantidades de prótons, nêutrons e elétrons dos elementos indicados pelos algarismos de I a V.
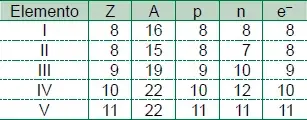
O elemento da tabela que possui a distribuição eletrônica 1s², 2s², 2p⁵ em seu estado fundamental é indicado por
- I.
- II.
- III.
- IV.
- V.
Resposta: C
Resolução: O elemento que possui distribuição eletrônica 1s², 2s², 2p⁵ em seu estado fundamental é o indicado por: III. Começa de 14:38
04. (Fuvest) Os elementos I, II e III têm as seguintes configurações eletrônicas em suas camadas de valência:
I – 3s² 3p³;
II – 4s² 4p⁵;
III – 3s².
Com base nessas informações, assinale a afirmação errada.
- O elemento I é um não-metal.
- O elemento II é um halogênio.
- O elemento III é um metal alcalino terroso.
- Os elementos I e III pertencem ao terceiro período da tabela periódica.
- Os três elementos pertencem ao mesmo grupo da tabela periódica.
Resposta: E
Resolução:
05. (CESMAC) Os implantes dentários são suportes metálicos posicionados cirurgicamente no osso maxilar, abaixo da gengiva, para posicionar corretamente as raízes dentárias. Por se tratar de um material leve, resistente e que apresenta mínima rejeição, o titânio (Ti) foi adotado como o principal material para a realização dos implantes dentários.
Considerando que o número atômico do Ti é 22, como se apresenta sua distribuição eletrônica?
- 1s² 2s² 2p⁶ 3s² 3p⁶ 3d⁴
- 1s² 2s² 2p⁶ 3s² 3p⁵ 3d⁵
- 1s² 2s² 2p⁶ 3s² 3p⁴ 3d⁴ 4s²
- 1s² 2s² 2p⁶ 3s² 3p⁶ 4s¹ 3d³
- 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d²
Resposta: E
Resolução: Para o titânio (Z = 22), a configuração eletrônica correta é: 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d².
06. (ACAFE) Considerando-se um elemento M genérico qualquer, que apresenta configuração eletrônica 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d⁵, pode-se afirmar que:
I. seu número atômico é 25;
II. possui 7 elétrons na última camada;
III. apresenta 5 elétrons desemparelhados;
IV. pertencem a família 7A.
Estão corretas as afirmações:
- I, II e III somente
- I e III somente
- II e IV somente
- I e IV somente
- II, III e IV somente
Resposta: B
Resolução: A afirmação correta com relação à configuração eletrônica (Z = 25) é: I e III estão corretas.
07. (EsPCEx) Considerando a distribuição eletrônica do átomo de bismuto (83Bi) no seu estado fundamental, conforme o diagrama de Linus Pauling, pode-se afirmar que seu subnível mais energético e o período em que se encontra na tabela periódica são, respectivamente:
- 5d⁵ e 5º período.
- 5d9 e 6º período.
- 6s² e 6º período.
- 6p⁵ e 5º período.
- 6p³ e 6º período.
Resposta: E
Resolução: O subnível mais energético do bismuto e o período correspondente são: 6p³ e 6º período.
08. (UDESC) Os elementos químicos sódio, ferro e fósforo são de grande importância para a sociedade, pois possuem inúmeras aplicações. Esses três elementos possuem a seguinte distribuição eletrônica:
Na – 1s² 2s² 2p⁶ 3s¹
Fe – 1s² 2s² 2p⁶ 3s2⁶ 4s² 3d⁶
P – 1s² 2s² 2p⁶ 3p³
A partir das distribuições eletrônicas acima, assinale a alternativa INCORRETA.
- O ferro é um elemento de transição interna.
- O fósforo é um elemento pertencente ao grupo do nitrogênio.
- O sódio é um metal alcalino.
- O fósforo é um não metal.
- O ferro é um metal.
Resposta: A
Resolução: O ferro é um elemento de transição externa, e não interna, portanto a afirmação incorreta é: O ferro é um elemento de transição interna.
09. (UP Medicina) De acordo com o modelo atômico de Rutherford-Böhr, o átomo de um elemento químico possui um núcleo com prótons e nêutrons e uma eletrosfera composta por várias camadas eletrônicas. Os elétrons se encontram distribuídos nas camadas eletrônicas de acordo com os subníveis de energia: s, p, d, f. Na formação dos íons, a distribuição eletrônica é alterada devido ao processo de ganho ou perda de elétrons.
(Números atômicos: Br = 35; K = 19)
No sal brometo de potássio, a distribuição eletrônica do ânion é:
- 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d¹0 4p⁴
- 1s² 2s² 2p⁶ 3s² 3p⁶ 4s¹
- 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d10 4p⁵
- 1s² 2s² 2p⁶ 3s² 3p⁶
- 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d10 4p⁶
Resposta: E
Resolução: A distribuição eletrônica correta para o ânion de brometo de potássio é: 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d¹⁰ 4p⁶.
10. (UFPA) O sódio (Na) é um metal alcalino presente no sal de cozinha. O número atômico do átomo de sódio é Z=11 e sua distribuição eletrônica é
- 1s² 2s³ 2p⁵ 3s¹
- 1s² 2s² 2p⁶ 3s¹
- 1s² 2s² 2p⁵ 3s²
- 1s² 2s⁴ 2p⁴ 3s¹
- 1s² 2s¹ 2p⁶ 3s²
Resposta: B
Resolução: A distribuição eletrônica correta para o sódio (Na) com Z=11 é: 1s² 2s² 2p⁶ 3s¹
11. (UP) Nos diferentes elementos químicos, a distribuição eletrônica representa o modo como os elétrons estão localizados pelas várias camadas ao redor do núcleo do átomo. No entanto, os elétrons não se distribuem aleatoriamente nessas camadas, pois existem algumas regras a serem seguidas para a representação do átomo no estado fundamental e de seus íons, assim como a distribuição dos elétrons nas camadas eletrônicas segue uma sequência crescente de subníveis de energia, nomeados como s, p, d, f. A seguir está representada a distribuição eletrônica de dois elementos químicos na forma de um cátion e de um ânion.
Cátion: 1s² 2s² 2p⁶ 3s² 3p⁶ Ânion: 1s² 2s² 2p⁶ 3s² 3p⁶
(Dados de alguns números atômicos: Na = 11; Cl = 17; K = 19; Ca = 20; Br = 35)
Assinale a alternativa que apresenta a fórmula molecular do sal composto pelo cátion e ânion cujas distribuições eletrônicas foram apresentadas acima.
- NaCl.
- CaCl2 .
- NaBr.
- CaBr2 .
- KBr.
Resposta: B
Resolução: A fórmula molecular do sal composto pelo cátion e ânion, com distribuições eletrônicas fornecidas (NaCl), é: CaCl₂
12. (UFPA) O Potássio (K; Z=19) é um elemento químico do grupo dos metais alcalinos. Sua distribuição eletrônica é
- 1s² 2s¹ 2p⁶ 3s² 3p7 4s¹
- 1s² 2s² 2p⁶ 3s³ 3p⁶
- 1s² 2s² 2p⁶ 3s² 3p⁶ 4s¹
- 1s² 2s² 2p⁶ 3s² 3p⁶ 3d¹
- 1s² 2s² 2p⁴ 3s³ 3p⁶ 4s²
Resposta: C
Resolução: A distribuição eletrônica correta para o potássio (K) com Z=19 é: 1s² 2s² 2p⁶ 3s² 3p⁶ 4s¹
13. (CESMAC) A deficiência de iodo no corpo humano pode causar diversos problemas de saúde, entre eles o bócio, que é o aumento no tamanho da glândula tireóide. No Brasil, desde agosto de 1953, é obrigatório que o sal de cozinha (cloreto de sódio) contenha sais de iodo, mais especificamente o iodato de potássio. Quais são, respectivamente, a distribuição eletrônica do íon K+ e a fórmula molecular do iodato de potássio?
Dado: número atômico do K = 19.
- 1s² 2s² 2p⁶ 3s² 3p⁶ 4s², KI
- 1s² 2s² 2p⁶ 3s² 3p⁶, KIO3
- 1s² 2s² 2p⁶ 3s² 3p⁶ 4s¹, KIO3
- 1s² 2s² 2p⁶ 3s² 3p⁶, KI
- 1s² 2s² 2p⁶ 3s² 3p⁶ 4s¹, KIO2
Resposta: B
Resolução: A distribuição eletrônica do íon K⁺ e a fórmula molecular do iodato de potássio são: 1s² 2s² 2p⁶ 3s² 3p⁶, KIO₃
14. (UNEMAT) O elemento químico Bromo é um não-metal com uma característica muito peculiar, que é o seu estado líquido quando em condiçõesambiente normais. É utilizado como agente sanitário no processo de purificação de águas, na indústria fotográfica, além de apresentar ação sedativa e antisséptica na área medicinal. É um halogênio pouco abundante e sua principal fonte de obtenção é a água do mar.
(Dados: Z=35)
Em relação ao Bromo, assinale a alternativa que representa corretamente sua distribuição eletrônica.
- 1s² 2s⁶ 2p² 3s⁶ 3p² 4s⁶ 3d10 4p¹
- 1s² 2s² 2p⁶ 3s² 3p⁶ 4s⁵ 3d10 4p²
- 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d10 4p⁵
- 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d8 4p7
- 1s6 2s² 2p² 3s⁶ 3p² 4s⁶ 3d10 4p¹
Resposta: C
Resolução: A distribuição eletrônica correta para o Bromo (Br) com Z=35 é: 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d¹⁰ 4p⁵
15. (UESC-BA) Os três elementos x, y e z têm as seguintes estruturas eletrônicas no estado fundamental:
x — 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d⁵
y — 1s² 2s² 2p⁶ 3s² 3p⁶
z — 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d10 4p⁴.
De acordo com tais estruturas, os três elementos podem ser classificados, respectivamente, como:
- elemento de transição, gás nobre, elemento representativo.
- elemento de transição, elemento representativo, gás nobre.
- elemento representativo, gás nobre, elemento de transição.
- elemento representativo, elemento de transição, gás nobre.
- gás nobre, elemento de transição, elemento representativo.
Resposta: A
Resolução: Classificação dos elementos com as estruturas fornecidas: elemento de transição, gás nobre, elemento representativo.
16. (IFRR) A distribuição eletrônica correta do elemento cobre é:
- [Ar] 4s² 3d9
- 1s² 2s² 2p⁶ 3s² 3p⁶ 4s¹ 3d10
- 1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d9
- 1s² 2s² 2p⁶ 3s² 3p⁶ 3d⁶
- [Ar] 3d6
Resposta: B
Resolução: A distribuição eletrônica correta para o cobre é: 1s² 2s² 2p⁶ 3s² 3p⁶ 4s¹ 3d¹⁰