CEDERJ 2021-2: Química
Gabarito: C
37. (CEDERJ 2021) Recentemente, em meio à busca por tratamentos que sejam eficazes no combate à infecção causada pelo Coronavírus SARS-CoV-2 (COVID-19), a Agência Nacional de Vigilância Sanitária (ANVISA) autorizou o uso do medicamento antiviral Remdesivir em pacientes, tornando-se este o primeiro medicamento a apresentar na bula a indicação de uso, e considerado promissor no combate à infecção, apesar do seu alto custo.
A estrutura da molécula do Remdesivir é apresentada a seguir.

Em relação à estrutura apresentada, é correto afirmar que
Dados: C=12, H=1, N=14, O=16, P=31
- os átomos de carbono presentes na estrutura apresentam hidridização do tipo sp3 ou sp2.
- a molécula apresenta as funções éster, amina, fenol, éter e nitrila.
- o Remdesivir apresenta massa molar igual a 602 g.mol-1.
- há seis átomos de carbono assimétricos na molécula do Remdesivir
Resolução: Começa Em: 01:34
Gabarito: A
38. (CEDERJ 2021) Suplementos minerais à base de zinco têm sido muito usados atualmente, em função da divulgação da ação deste elemento no organismo com efeito de auxílio no fortalecimento do sistema imunológico. Um dos tipos de suplementos vendidos é o ZMC, suplemento que, além de zinco, apresenta magnésio e vitamina C na sua composição.
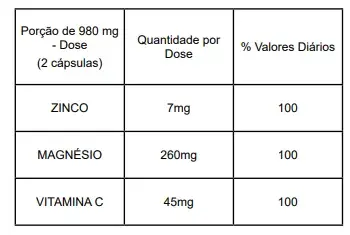
A seguir é mostrada a tabela de informações nutricionais presente em um frasco de ZMC:
Considerando que zinco metálico puro reagiu completamente com 200mL de solução 1,0 mol.L-1 de ácido clorídrico e que todo o íon zinco resultante, após tratamento adequado para eliminação de impurezas, foi usado para a produção de frascos de ZMC com 90 cápsulas cada um, com a composição citada na tabela, a quantidade máxima de frascos que se pode produzir é
Dados: Zn=65,4, H=1, Cl=35,5
- 20.
- 10.
- 25.
- 15.
Resolução: Começa Em: 06:30
Gabarito: B
39. (CEDERJ 2021) O monóxido de carbono e o dióxido de nitrogênio são gases muito tóxicos, capazes de levar à morte ao serem inalados, principalmente o monóxido, pois é incolor e inodoro, sendo inalado sem que se perceba, enquanto o dióxido de nitrogênio é um gás castanho, de odor forte e irritante das vias aéreas e respiratórias. Esses gases podem reagir entre si, a 540K, produzindo dióxido de carbono e óxido nítrico, gases menos tóxicos, conforme a equação a seguir.

A reação teve sua cinética estudada e os dados obtidos em alguns experimentos estão indicados na tabela abaixo

Em relação ao que foi descrito, é correto concluir que a reação apresenta
- cinética de 1ª ordem global, e a constante de velocidade é igual a 3,23.10-2.
- cinética de 2ª ordem global, e a constante de velocidade é igual a 3,23.10-2.
- cinética de 1ª ordem global, e a constante de velocidade é igual a 1,75.10-3.
- cinética de 2ª ordem global, e a constante de velocidade é igual a 1,75.10-3.
Resolução: Começa Em: 14:00
Gabarito: ANULADA
40. (CEDERJ 2021) A osmose é, para os organismos, a mais importante das propriedades coligativas, pois as paredes das células agem como membranas semipermeáveis, permitindo e selecionando a troca de matéria com o meio extracelular, em função da concentração dos meios (conceitos de hipertônico e hipotônico).
Nesse sentido, 500mL de uma solução aquosa de manitol (isômero da glicose – C6 H12O6) deve ser administrada por um veterinário em um cão que passará por tratamento neurológico, a fim de tentar diminuir a pressão intracraniana, devido à sua ação diurética por osmose. Sabendo que o sangue tem pressão osmótica de 7,6atm, a 38ºC (temperatura corporal do cão), e que a solução injetada deve ser isotônica ao sangue do animal, a concentração da solução de manitol a ser injetada deve ser, em mol.L-1, aproximadamente igual a
- 0,25.
- 0,15.
- 1,5.
- 2,5.
Resolução: Começa Em: 26:50
Gabarito: A
41. (CEDERJ 2021) O segundo postulado da teoria atômica de Dalton estabelecia que “átomos de um mesmo elemento químico são idênticos e iguais em peso”. Por mais de um século essa concepção foi hegemônica, o que levou a um problema, aparentemente sem solução, relacionado à determinação das massas atômicas dos elementos químicos, cujos valores variavam de um experimento para outro. O surgimento da espectrometria de massas, no início do Século XX, solucionou o problema com a grande contribuição de Francis W. Aston, que recebeu o Prêmio Nobel de Química em 1922. A técnica analítica consiste em separar íons no estado gasoso, por meio da relação massa/carga de átomos e moléculas. Tal ferramenta permitiu a determinação precisa das massas atômicas dos elementos.
O desenvolvimento da espectrometria de massas levou à confirmação da existência dos
- isótopos, que são átomos de um mesmo elemento que possuem diferentes números de nêutrons, tendo, assim, relação carga/massa diferentes.
- isótonos, que são átomos de um mesmo elemento que possuem mesmo número de nêutrons, tendo, assim, relação carga/massa diferentes.
- isóbaros, que são átomos de um mesmo elemento que possuem mesmo número de massa, tendo, assim, relação carga/massa diferentes.
- isoeletrônicos, que são átomos e íons de um mesmo elemento que possuem mesmo números de elétrons, tendo, assim, relação carga/massa diferentes.
Resolução: Começa Em: 30:50
Gabarito: C
42. (CEDERJ 2021) O luminol (5-amino-2,3-di-hidro-1,4-ftalazinadiona) é muito utilizado em perícias criminais a fim de identificar a presença de sangue em locais de crimes contra pessoas, mesmo que o local tenha sido lavado, sendo uma ferramenta muito útil no auxílio ao trabalho pericial. A ação do luminol ocorre por meio de uma reação de quimiluminescência na presença de peróxido de hidrogênio em meio básico, catalisada pelo íon ferro presente na hemoglobina, emitindo luz de cor azul e revelando as manchas de sangue. A reação, de forma simplificada, é representada a seguir.

Em relação a esta reação, pode-se afirmar corretamente que
- O luminol é o agente oxidante na reação.
- O íon ferro da hemoglobina é consumido, já que sofre oxidação, pois o catalisador também participa da reação.
- O íon ferro da hemoglobina acelera a reação entre o luminol e o peróxido ao diminuir a energia de ativação da reação.
- O peróxido de hidrogênio é o agente redutor da reação.
Resolução: Começa Em: 32:55